El promedio global de personas vive 9,6 años con discapacidad significativa antes de morir. No con achaques leves. Con limitaciones funcionales reales: dificultad para caminar, dependencia parcial, declive cognitivo. La medicina del siglo XX logró que viviéramos más — una hazaña extraordinaria. Pero una proporción creciente de esos años adicionales se vive con enfermedad crónica controlada, no curada.
Esta es la paradoja del envejecimiento moderno: el éxito que reveló el siguiente problema.
La distinción entre lifespan (esperanza de vida total) y healthspan (años vividos con salud funcional) no es un tecnicismo. Es la diferencia entre dos objetivos completamente distintos para la medicina preventiva, para las decisiones de salud individuales y para las políticas públicas. Sin claridad sobre cuál de los dos estamos intentando optimizar, cualquier conversación sobre longevidad carece de norte.
En este artículo revisamos qué sabemos con certeza científica, qué es probable pero requiere matices, y — esto es crucial — qué permanece genuinamente incierto. Cada afirmación lleva su grado de evidencia explícito.
Los dos conceptos que definen cómo envejecemos
Lifespan: los años totales
El lifespan es simplemente la duración total de vida, medida desde el nacimiento hasta la muerte. A nivel poblacional se expresa como esperanza de vida: el número promedio de años que se espera que viva una persona nacida en un año determinado, bajo condiciones de mortalidad actuales.
Los datos demográficos documentan un incremento notable. Según el Global Burden of Disease Study 2021, la esperanza de vida mundial pasó de aproximadamente 48 años en 1950 a 73 años en 2019. [[1]] Este progreso refleja avances fundamentales: reducción de mortalidad infantil, control de enfermedades infecciosas, mejoras en nutrición, tratamientos efectivos para condiciones agudas que antes eran mortales.
Esta métrica, sin embargo, no distingue entre años vividos con salud plena y años vividos con enfermedad o discapacidad. Dos personas pueden compartir la misma esperanza de vida de 80 años y haber experimentado trayectorias totalmente diferentes de salud funcional.
Healthspan: los años funcionales
El healthspan representa los años vividos libres de enfermedad crónica mayor y discapacidad funcional significativa. Conviene separar este concepto de nociones vagas de "bienestar": no implica ausencia total de cualquier condición médica, sino preservación de funcionalidad y autonomía en las actividades diarias.
La medición operativa se realiza mediante varios indicadores:
DALYs (Disability-Adjusted Life Years): años de vida ajustados por discapacidad, que combinan años perdidos por muerte prematura con años vividos con limitaciones funcionales.
Autoreporte funcional: capacidad para realizar actividades básicas (caminar, vestirse, alimentarse) e instrumentales (gestionar finanzas, cocinar, usar transporte) de forma independiente.
Independencia en actividades diarias: medida clínica de autonomía física y cognitiva.
La Organización Mundial de la Salud utiliza el concepto de "esperanza de vida saludable" (Healthy Life Expectancy, HALE), que cuantifica los años esperados vividos en plena salud. Según datos de 2019, mientras la esperanza de vida global era de 73.3 años, el HALE era de 63.7 años, revelando una brecha promedio de 9.6 años [[2]]
La distinción que cambia el objetivo
Confundir ambos conceptos distorsiona fundamentalmente nuestros objetivos en salud. Cuando alguien habla de "longevidad" sin especificar, ¿se refiere a vivir más años, o a vivir más años con funcionalidad preservada? La respuesta importa.
Considere dos escenarios:
Persona A vive hasta los 85 años, pero desarrolla diabetes tipo 2 a los 55, enfermedad cardiovascular a los 62, y experimenta 15 años de multimorbilidad severa con movilidad limitada, dependencia parcial para actividades diarias y declive cognitivo progresivo.
Persona B vive hasta los 80 años, mantiene funcionalidad completa hasta los 78, y experimenta solo dos años de declive antes de morir.
Desde la perspectiva del lifespan, la persona A "vivió más." Desde la perspectiva del healthspan, la persona B preservó autonomía y funcionalidad durante una proporción mucho mayor de su vida.
Esta distinción no implica un juicio sobre cuál vida tiene más valor—la calidad de vida es multidimensional y subjetiva, y muchas personas con condiciones crónicas reportan satisfacción vital alta—. Lo que clarifica es qué estamos intentando optimizar cuando hablamos de envejecimiento saludable. Y esa claridad precede cualquier decisión informada.
La brecha de 9,6 años: qué dicen los datos globales
Evidencia del Global Burden of Disease 2021
Los datos epidemiológicos globales documentan con solidez la existencia y magnitud del gap entre healthspan y lifespan. El Global Burden of Disease Study 2021, que analiza datos de 204 países, reporta que el promedio global vive entre 8 y 12 años con discapacidad significativa antes de morir.
Este fenómeno no es estático. Durante las últimas tres décadas, tanto el lifespan como los años con discapacidad han aumentado en términos absolutos. Entre 1990 y 2019, los años de vida perdidos por discapacidad aumentaron un 34% a nivel global. [[1]] En países de ingresos altos, donde el lifespan es mayor, este gap tiende a ser más pronunciado.
Un análisis publicado en The Lancet (2020) que examinó tendencias en 195 países encontró que aunque la esperanza de vida aumentó 6.5 años entre 2000 y 2019, la esperanza de vida saludable solo aumentó 5.4 años, ampliando el gap en más de un año durante ese periodo. [[3]] No estamos cerrando la brecha—la estamos ensanchando.
Estudios longitudinales de cohortes específicas confirman este patrón. El Framingham Heart Study, que ha seguido a múltiples generaciones desde 1948, documenta que las generaciones más recientes viven más años pero también experimentan más años con enfermedades cardiovasculares controladas pero no curadas. [[4]] El UK Biobank, con más de 500,000 participantes, reporta incremento en la prevalencia de multimorbilidad (dos o más enfermedades crónicas) en personas mayores de 65 años, llegando al 65% en ese grupo etario. [[5]]
EVIDENCIA CLAVE · GRADO A
La brecha entre esperanza de vida y esperanza de vida saludable (HALE) alcanzaba los 9,6 años de promedio global en 2019: 73,3 años de vida total frente a 63,7 años vividos con funcionalidad plena. Esta diferencia no se está cerrando — entre 1990 y 2019, los años de vida perdidos por discapacidad aumentaron un 34% a nivel mundial.
La desigualdad oculta: el gap es mayor en países ricos
Los promedios globales ocultan heterogeneidad significativa. El gap healthspan-lifespan varía considerablemente por región geográfica, nivel socioeconómico y características individuales —y esta variación contiene información crucial.
Variabilidad geográfica: Algunos países nórdicos (Noruega, Suecia) muestran evidencia de compresión relativa de morbilidad, con gaps más estrechos entre esperanza de vida y esperanza de vida saludable. [[6]] En contraste, países de ingresos medios que han experimentado transición epidemiológica rápida —aumento de enfermedades crónicas con infraestructura sanitaria insuficiente— muestran gaps más amplios. La geografía no es destino, pero estructura posibilidades.
Desigualdades socioeconómicas: Un meta-análisis de 48 estudios publicado en JAMA Internal Medicine (2021) encontró que las personas en el quintil socioeconómico más bajo experimentan en promedio 5-7 años menos de healthspan comparado con el quintil más alto, incluso cuando el lifespan solo difiere 3-4 años. [[7]] El nivel educativo, el acceso a atención médica preventiva, las condiciones laborales y el ambiente físico contribuyen a esta disparidad. La desigualdad en healthspan es más pronunciada que la desigualdad en lifespan.
La paradoja de género
Las mujeres tienden a vivir más años que los hombres (lifespan mayor), pero también experimentan más años con discapacidad, resultando en un gap healthspan-lifespan más amplio. [[8]]
Esto se denomina la "paradoja de supervivencia femenina"—vivir más no garantiza vivir mejor funcionalmente.
Rango individual
Existe un espectro amplio en la experiencia individual. Algunos experimentan muerte súbita mientras mantienen funcionalidad completa. Otros viven 20 o más años con limitaciones severas progresivas. Los promedios poblacionales no predicen trayectorias individuales con certeza—y esta incertidumbre es genuina, no simplemente una limitación de medición.
Casos excepcionales no son la norma
Los medios frecuentemente destacan casos de centenarios que mantienen funcionalidad notable hasta edades muy avanzadas. Estos casos existen: el fenómeno de "superenvejecimiento" está documentado en poblaciones específicas (zonas azules, ciertos grupos familiares con longevidad excepcional).
Pero representan valores atípicos estadísticos extremos. Menos del 0.01% de la población mundial llega a los 100 años, y una fracción aún menor mantiene funcionalidad completa. [[9]] Los mecanismos de esta excepcionalidad involucran combinaciones raras de factores genéticos protectores, historia de exposiciones favorables y, probablemente, elementos estocásticos que no comprendemos completamente.
Presentar estos casos como modelo generalizable para la población general es epidemiológicamente incorrecto y genera expectativas irrealistas. El sesgo de supervivencia —solo vemos a quienes llegaron a edades extremas en buen estado— oculta la mayoría silenciosa que no lo logró. Esta no es una observación cínica; es una lectura honesta de los datos disponibles.
Por qué se amplía la brecha en lugar de cerrarse
El éxito parcial de la medicina moderna
El gap healthspan-lifespan no resulta de un fracaso médico, sino de un progreso parcial con desafíos pendientes. Esta distinción importa para orientar correctamente la investigación y las políticas de salud futuras.
La medicina del siglo XX logró reducciones masivas en mortalidad aguda e infantil. Las enfermedades infecciosas que antes mataban en días o semanas —neumonía, infecciones bacterianas, tuberculosis— se volvieron tratables con antibióticos. Las vacunas eliminaron o redujeron drásticamente enfermedades como polio, sarampión y viruela. La mortalidad infantil en países de ingresos altos cayó de más del 20% a menos del 0.5%. [[1]]
Para enfermedades crónicas mayores —cardiovasculares, diabetes, muchos cánceres— la medicina desarrolló tratamientos efectivos para control, no curación. Las estatinas reducen colesterol y previenen eventos cardiovasculares. Los inhibidores de la ECA y betabloqueadores controlan presión arterial. La insulina y antidiabéticos orales gestionan glucosa. La quimioterapia y terapias dirigidas extienden supervivencia en cáncer.
El resultado: más personas sobreviven a eventos que antes eran mortales y viven décadas con condiciones crónicas controladas farmacológicamente. Un infarto que en 1950 mataba en el 40% de casos ahora tiene mortalidad hospitalaria menor al 5%. [[10]] Pero el 95% que sobrevive frecuentemente continúa con función cardiaca reducida, requiere múltiples medicamentos y enfrenta riesgo elevado de eventos subsecuentes.
Esto es progreso genuino—sobrevivir es preferible a morir—pero revela el siguiente nivel del desafío: ¿Cómo prevenir la incidencia inicial de estas condiciones en lugar de solo gestionarlas una vez establecidas?
Hasta aquí llega lo que la medicina actual hace excepcionalmente bien. Lo que sigue requiere un enfoque diferente.
Multimorbilidad: cuando las enfermedades se multiplican
La multimorbilidad —presencia simultánea de dos o más enfermedades crónicas— se ha convertido en la norma, no la excepción, en personas mayores de 65 años en países de ingresos altos.
Datos del National Health and Nutrition Examination Survey (NHANES) en Estados Unidos muestran que el 68% de adultos mayores de 65 años tienen al menos dos condiciones crónicas, y el 36% tienen cuatro o más. [[11]] El UK Biobank reporta prevalencias similares. [[5]] No estamos hablando de casos aislados.
La multimorbilidad tiene efectos compuestos no aditivos. La diabetes no solo afecta el control glucémico; aumenta riesgo cardiovascular, daña función renal, compromete cicatrización y acelera declive cognitivo. La enfermedad cardiovascular interactúa con enfermedad renal crónica en ciclos de deterioro mutuo. La presencia de múltiples condiciones complica el tratamiento —polifarmacia, interacciones medicamentosas— y acelera el declive funcional más que la suma de condiciones individuales.
Un estudio longitudinal publicado en BMJ (2019) siguió a más de 1.75 millones de personas durante 15 años y encontró que cada condición crónica adicional después de la primera aceleraba el declive funcional en un 30-40% más de lo esperado por efecto aditivo simple. [[12]] Las enfermedades no suman—interactúan.
Factores de riesgo persistentes
Aunque comprendemos mejor los factores de riesgo para enfermedades crónicas, muchos muestran prevalencia creciente o persistentemente alta en poblaciones globales.
Obesidad: La prevalencia global de obesidad se ha triplicado desde 1975. En 2016, el 39% de adultos tenía sobrepeso y el 13% obesidad. [[13]] La obesidad está fuertemente asociada con diabetes tipo 2, enfermedad cardiovascular, ciertos cánceres, osteoartritis y mortalidad prematura.
Sedentarismo: Más del 25% de la población adulta global no cumple con niveles mínimos recomendados de actividad física. [[14]] El trabajo sedentario, urbanización y tecnología han reducido el gasto energético diario promedio significativamente.
Dieta procesada: El consumo de alimentos ultraprocesados ha aumentado globalmente, particularmente en países de ingresos medios experimentando transición nutricional. Estudios observacionales grandes asocian mayor consumo de ultraprocesados con incremento en mortalidad cardiovascular y por todas las causas. [[15]]
Exposiciones ambientales: Contaminación del aire, disruptores endocrinos, microplásticos y otros contaminantes emergentes muestran asociaciones con enfermedades crónicas, aunque la magnitud del efecto causal es difícil de cuantificar.
Conviene enfatizar: estos factores muestran correlación fuerte con reducción de healthspan en estudios observacionales de largo plazo, pero la causalidad completa no está establecida de manera definitiva. Realizar ensayos controlados aleatorizados de 40 años es imposible por razones éticas y prácticas. Múltiples factores confusores —nivel socioeconómico, acceso a atención médica, factores genéticos, otras exposiciones— dificultan aislar efectos causales puros.
Sin embargo, la consistencia de asociaciones a través de múltiples estudios, poblaciones y diseños metodológicos proporciona confianza razonable en estas relaciones. La evidencia no es perfecta, pero es la mejor disponible. Y apunta en una dirección clara.
El healthspan no depende solo de ti: determinantes sociales
Acceso desigual a recursos para vivir mejor
El healthspan no es primariamente resultado de elecciones individuales. Esta afirmación merece detenimiento porque contradice narrativas populares sobre "responsabilidad personal" en salud. Los datos muestran que el healthspan está profundamente determinado por factores estructurales y acceso a recursos.
El nivel socioeconómico determina acceso a:
Alimentación nutritiva: Los alimentos frescos, no procesados y ricos en nutrientes son significativamente más caros por caloría que alimentos ultraprocesados. En muchos contextos urbanos de bajos recursos, el acceso físico a supermercados con productos frescos es limitado— los llamados "desiertos alimentarios."
Tiempo y espacio para ejercicio: El ejercicio regular requiere tiempo libre, que no está disponible para personas con múltiples empleos o responsabilidades de cuidado no remuneradas. Requiere también acceso a espacios seguros: parques, gimnasios, vecindarios transitables. Estos recursos están desigualmente distribuidos.
Atención médica preventiva: Aunque el tratamiento de emergencia puede estar disponible, el acceso a medicina preventiva de calidad —chequeos regulares, screening temprano, especialistas— está estratificado por capacidad de pago y tipo de seguro.
Educación sobre salud: El nivel educativo correlaciona fuertemente con alfabetización en salud (health literacy), capacidad de interpretar información médica y tomar decisiones informadas.
Un análisis del Nurses' Health Study y Health Professionals Follow-up Study publicado en Circulation (2018) encontró que el gradiente socioeconómico en healthspan es más pronunciado que el gradiente en lifespan. Las personas en el quintil socioeconómico más bajo vivían 3-4 años menos, pero experimentaban 6-8 años menos de vida libre de enfermedad crónica. [[16]]
Esta disparidad no se explica completamente por diferencias en comportamientos individuales. Incluso cuando se controla estadísticamente por dieta, ejercicio, tabaco y alcohol, persiste una asociación independiente entre nivel socioeconómico y healthspan, sugiriendo que el estrés crónico, la calidad ambiental, la seguridad laboral y otros factores estructurales contribuyen directamente. [[17]]
Factores estructurales que impactan el healthspan
La Esperanza de Vida Saludable/Funcional requiere tiempo, acceso a información, recursos financieros y un ambiente que permita implementar cambios sostenibles.
Factores estructurales que impactan healthspan pero están fuera del control individual incluyen:
Diseño urbano: La "transitabilidad" de vecindarios —presencia de aceras, parques, iluminación, seguridad percibida— correlaciona con niveles de actividad física y salud cardiovascular. [[18]] Las personas no eligen si su vecindario tiene parques o es seguro caminar de noche.
Políticas públicas: Regulaciones sobre etiquetado de alimentos, impuestos a productos no saludables, subsidios agrícolas, acceso a atención médica universal versus sistema basado en seguros privados —todas estas decisiones políticas estructuran el ambiente de decisiones individuales.
Condiciones laborales: Horarios excesivos, trabajo por turnos que disrumpe ritmos circadianos, exposiciones ocupacionales (químicos, ruido, estrés), inseguridad laboral —estos factores impactan salud independientemente de "elecciones" individuales sobre dieta o ejercicio.
Educación temprana: La exposición a educación sobre salud durante la infancia y adolescencia establece trayectorias de largo plazo. Esta educación está desigualmente distribuida.
Reconocer estos determinantes sociales no es excusa para la inacción individual dentro de las circunstancias de cada persona, sino que es el contexto necesario para evitar la culpabilización simplista. El mensaje "tu healthspan depende de tus elecciones" es teóricamente falso y éticamente problemático cuando ignora estas realidades estructurales.
¿Se puede comprimir la morbilidad? Evidencia sólida dice que sí
Qué demuestran los estudios longitudinales de largo plazo
La compresión de morbilidad —concepto introducido por James Fries en 1980— se refiere a retrasar el inicio de discapacidad y enfermedad crónica hacia etapas más tardías de la vida, reduciendo así el tiempo total vivido con limitaciones funcionales.
La evidencia longitudinal robusta demuestra que esto es alcanzable a nivel poblacional e individual. No es especulación teórica.
El Harvard Alumni Health Study siguió a más de 17,000 graduados desde los años 1960 hasta su muerte o hasta 2012. Encontró que aquellos que mantuvieron actividad física regular y no fumaron retrasaron el inicio de discapacidad significativa en un promedio de 5 años comparado con personas sedentarias o fumadoras, sin diferencia sustancial en edad de muerte. [[19]] Resultado: compresión del periodo de discapacidad.
El Nurses' Health Study, que ha seguido a más de 120,000 enfermeras desde 1976, reportó hallazgos similares. En análisis publicados en BMJ (2020), las mujeres que mantenían cinco factores de bajo riesgo —no fumar, peso saludable, ejercicio regular, dieta de calidad, consumo moderado o nulo de alcohol— vivían en promedio 7.6 años más libres de enfermedad crónica mayor comparado con mujeres sin ninguno de estos factores. [[20]]
Crucialmente, estos estudios miden no solo incidencia de enfermedad sino también funcionalidad mantenida.
El concepto relevante es "años libres de discapacidad", no solo ausencia de diagnóstico médico.
Datos poblacionales de algunos países también sugieren compresión de morbilidad agregada. Análisis de tendencias en Estados Unidos y varios países europeos muestran que, aunque el lifespan ha aumentado, la edad promedio de inicio de limitaciones funcionales también ha aumentado, en algunos casos más rápido que el aumento en longevidad. [[21]]
La compresión de morbilidad no es universal ni garantizada, pero es un objetivo biológicamente plausible y evidenciado en subpoblaciones. Esta posibilidad fundamenta racionalmente el enfoque de Muana Lab.
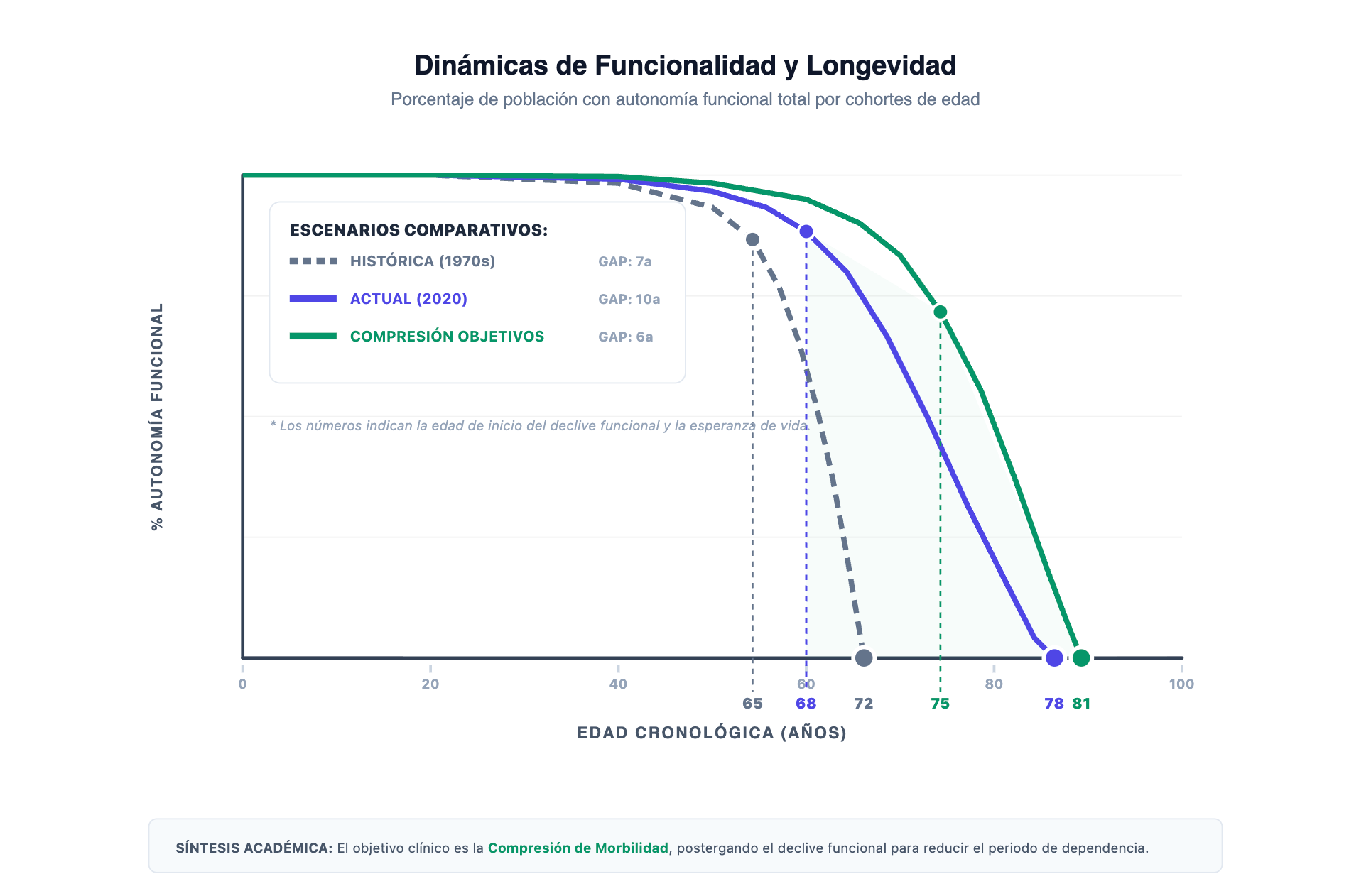
EVIDENCIA CLAVE · GRADO A
La compresión de morbilidad — retrasar el inicio de la discapacidad hacia las etapas finales de la vida — está documentada en estudios longitudinales robustos. El Harvard Alumni Health Study encontró que mantener actividad física regular y no fumar retrasó el inicio de discapacidad en un promedio de 5 años, sin diferencia en edad de muerte.
Factores con mayor evidencia científica
Los estudios observacionales de largo plazo identifican consistentemente ciertos factores asociados con mayor healthspan. Conviene ser explícitos sobre lo que esta evidencia significa y lo que no significa.
La evidencia más robusta existe para actividad física. Un meta-análisis de 44 estudios de cohortes publicado en BMJ (2019) encontró que niveles más altos de actividad física se asociaban con reducción del 30-40% en riesgo de mortalidad prematura y del 20-35% en riesgo de enfermedades cardiovasculares, diabetes tipo 2 y ciertos cánceres. [[22]]
El ejercicio que combina entrenamiento cardiovascular y de resistencia muestra las asociaciones más fuertes con preservación de funcionalidad en edad avanzada. El entrenamiento de resistencia previene sarcopenia —pérdida de masa muscular— y mantiene fuerza, predictores importantes de independencia funcional. [[23]]
Las guías de la OMS recomiendan 150-300 minutos semanales de actividad aeróbica moderada o 75-150 minutos de actividad vigorosa, más dos sesiones semanales de entrenamiento de resistencia. [[24]]
Patrón alimentario no procesado:
No existe una dieta única "óptima" respaldada por evidencia definitiva. Sin embargo, varios patrones alimentarios muestran asociaciones consistentes con mejor healthspan:
- La dieta mediterránea: meta-análisis de estudios observacionales y ensayos clínicos asocian adherencia a este patrón con reducción del 25% en riesgo cardiovascular y del 10-15% en mortalidad por todas las causas. [[25]]
- La dieta DASH: desarrollada para control de hipertensión, muestra beneficios cardiovasculares y reducción de riesgo de diabetes. [[26]]
- Patrones plant-forward: mayor consumo de alimentos vegetales integrales—frutas, verduras, legumbres, granos integrales, nueces— y menor consumo de carnes rojas y procesadas se asocia consistentemente con mejor salud cardiometabólica. [[27]]
Un denominador común emerge: minimizar ultraprocesados.
Estudios de cohortes grandes asocian mayor consumo de ultraprocesados con incremento en riesgo cardiovascular y mortalidad [[15]].
Sueño consistente:
Meta-análisis de estudios prospectivos encuentran una relación en forma de U entre duración de sueño y mortalidad/morbilidad. Tanto sueño insuficiente (menos de 6 horas) como excesivo (más de 9 horas) se asocian con mayor riesgo cardiovascular y metabólico. El rango óptimo aparece entre 7-8 horas por noche con regularidad [[28]].
La calidad del sueño —continuidad, arquitectura de fases— también importa, no solo duración. Trastornos del sueño como apnea obstructiva están independientemente asociados con riesgo cardiovascular y metabólico.
No tabaco, alcohol limitado:
El tabaquismo tiene las asociaciones más fuertes y consistentes con reducción tanto de lifespan como healthspan. Dejar de fumar en cualquier edad muestra beneficios sustanciales. [[29]]
Para alcohol, la evidencia es más compleja. Consumo moderado (1 bebida/día para mujeres, 1-2 para hombres) mostró en estudios observacionales asociación con menor riesgo cardiovascular comparado con no bebedores, pero estudios recientes con metodologías más rigurosas sugieren que beneficios pueden ser artefacto de confusión —los "no bebedores" frecuentemente incluyen ex-bebedores con problemas de salud. El consenso actual se inclina hacia: si no bebes, no hay razón basada en evidencia para empezar; si bebes, limitar consumo es prudente. [[30]]
Conexión social significativa:
Meta-análisis de 148 estudios (más de 300,000 participantes) encontró que personas con relaciones sociales más fuertes tenían 50% mayor probabilidad de supervivencia durante los periodos de seguimiento comparado con aquellas con relaciones más débiles. [[31]] El aislamiento social y la soledad se asocian con incremento en mortalidad comparable al tabaquismo o la obesidad.
| Factor | Evidencia | Efecto documentado |
|---|---|---|
| Ejercicio regular (cardio + fuerza) | Grado A — meta-análisis 44 cohortes (BMJ 2019) | ↓30-40% mortalidad prematura |
| Patrón alimentario no ultraprocesado | Grado A — Nurses' Health Study | +7,6 años libres de enfermedad |
| Sueño consistente 7-8h | Grado A — curva U documentada | Menor riesgo CV y metabólico |
| No fumar | Grado A — evidencia más sólida | Mayor impacto individual documentado |
| Conexión social significativa | Grado A — meta-análisis 148 estudios | +50% probabilidad supervivencia |
Guía Técnica de Niveles de Evidencia
| Nivel | Nombre | Estudios | Significado |
|---|---|---|---|
| A | Evidencia Alta/Muy Alta | Metaanálisis, revisiones sistemáticas o ECA de alta calidad | Conclusión sólida. Confianza alta en que el efecto sea el verdadero |
| B | Moderada/Baja | ECA con limitaciones, estudios de cohorte o casos y controles | Evidencia orientativa. Probable efecto verdadero con incertidumbre |
| C | Baja/Opinión | Estudios descriptivos no experimentales o series de casos | Evidencia limitada o débil. Basado en experiencia clínica o consenso |
| D | Muy Baja/Opinión | Estudios descriptivos no experimentales o series de casos | Evidencia limitada o débil. Basado en experiencia clínica o consenso |
Matiz crítico obligatorio sobre todos estos factores:
Estos hallazgos provienen de estudios observacionales de largo plazo. Realizar ensayos controlados aleatorizados de 30-40 años siguiendo personas desde edad adulta joven hasta muerte es imposible práctica y éticamente. Por tanto, aunque las asociaciones son fuertes, consistentes a través de múltiples estudios y poblaciones, y biológicamente plausibles, no podemos afirmar causalidad con el mismo nivel de certeza que tendríamos con evidencia experimental.
Además, múltiples factores confusores persisten: las personas que ejercitan regularmente también tienden a tener mayor nivel educativo, mejor acceso a atención médica, trabajos menos físicamente destructivos y otros factores protectores. Los análisis estadísticos intentan controlar estos confusores, pero el control perfecto es imposible.
La evidencia apoya razonablemente que estos factores tienen efectos causales reales sobre healthspan, pero la magnitud exacta del efecto y la aplicabilidad individual permanecen inciertos. Esta incertidumbre residual no es falta de rigor—es reconocimiento honesto de los límites del conocimiento actual.
Intervenciones médicas preventivas con respaldo
Más allá de factores de estilo de vida, ciertas intervenciones médicas tienen evidencia de impacto en healthspan.
Control de factores de riesgo cardiovascular:
El tratamiento de hipertensión, hipercolesterolemia y diabetes reduce incidencia de eventos cardiovasculares mayores —infarto, ACV— en ensayos clínicos aleatorizados. [[32]] [[33]] [[34]] Reducir eventos cardiovasculares claramente impacta healthspan: un infarto frecuentemente resulta en discapacidad funcional permanente.
Sin embargo, el impacto en años funcionales totales es menos claro. Los estudios miden típicamente eventos cardiovasculares y mortalidad, menos frecuentemente funcionalidad mantenida hasta edad avanzada. El efecto neto —prevenir eventos pero potencialmente extender vida con otras condiciones crónicas— requiere estudios de seguimiento muy largo que son escasos.
Vacunación:
Las vacunas contra influenza, neumococo y herpes zóster en adultos mayores reducen incidencia de infecciones que pueden precipitar declive funcional. La influenza y neumonía son causas mayores de hospitalización y pérdida de funcionalidad en mayores de 65 años. [[35]]
Screening oncológico selectivo:
Screening de cáncer colorrectal —colonoscopia, test de sangre oculta en heces— reduce mortalidad por cáncer colorrectal en ensayos aleatorizados. [[36]] Mamografía para cáncer de mama muestra beneficio en mujeres 50-74 años, aunque la magnitud es debatida. [[37]] Otros screenings (próstata, pulmón en fumadores de alto riesgo) tienen evidencia más limitada o controversial.
El screening debe balancear beneficio —detectar cáncer temprano— con daños: sobrediagnóstico, procedimientos innecesarios, ansiedad. Las recomendaciones son específicas por edad y perfil de riesgo.
Estas intervenciones tienen evidencia sólida para reducción de morbilidad específica, pero el impacto agregado en healthspan total —considerando efectos sobre funcionalidad multidimensional hasta final de vida— es difícil de cuantificar con precisión. Esta dificultad no invalida las intervenciones, pero limita nuestras afirmaciones sobre su alcance.
Fronteras del conocimiento: qué aún no sabemos
Biomarcadores de "edad biológica": promesa vs. realidad
Una promesa atractiva de la medicina de precisión es poder medir "edad biológica" individual y predecir trayectorias de envejecimiento antes de que aparezcan síntomas clínicos. Esta promesa permanece, hasta ahora, principalmente no cumplida.
Telómeros:
Los telómeros —secuencias repetitivas en extremos de cromosomas que se acortan con cada división celular— se propusieron como biomarcador de envejecimiento. La longitud telomérica promedio en leucocitos correlaciona débilmente con edad cronológica y se asocia modestamente con mortalidad en meta-análisis [[38]].
Sin embargo, la variabilidad individual es enorme, la medición está sujeta a error técnico significativo, y no existen intervenciones validadas para "alargar" telómeros con impacto demostrado en healthspan. Las pruebas comerciales de telómeros carecen de utilidad clínica establecida. Comprar esa prueba no te dice qué hacer diferente.
Relojes epigenéticos:
Los patrones de metilación del ADN cambian predeciblemente con edad. Algoritmos como el "reloj de Horvath" predicen edad cronológica con error promedio de 3-4 años basándose en metilación. [[39]] Versiones más recientes (GrimAge, PhenoAge) predicen mortalidad y riesgo de enfermedad mejor que edad cronológica sola.
Esto es prometedor, pero la validez clínica no está establecida. ¿Qué hacer con la información de que tu "edad epigenética" es 5 años mayor que tu edad cronológica? No hay intervenciones probadas para "revertir" edad epigenética, y no está claro si hacerlo sin cambiar factores subyacentes tendría beneficio real.
Proteómica y metabolómica:
Perfiles de proteínas circulantes y metabolitos muestran asociaciones con envejecimiento y riesgo de enfermedad. Algunos paneles comerciales prometen predicción de riesgo personalizada. La investigación es activa pero la utilidad clínica está en desarrollo.
Actualmente, no existe un biomarcador validado y accionable de "edad biológica" que justifique modificar decisiones clínicas más allá de factores de riesgo tradicionales —presión arterial, glucosa, lípidos, IMC. Esta es una frontera genuina del conocimiento, no simplemente una laguna temporal que pronto se llenará.
Intervenciones emergentes sin evidencia humana suficiente
La biología del envejecimiento está avanzando rápidamente, pero la mayor parte de la investigación emocionante permanece en fase preclínica. La distancia entre roedores y humanos es mayor de lo que narrativas populares sugieren.
Senolíticos:
Las células senescentes —células que han dejado de dividirse pero no mueren— se acumulan con edad y secretan factores inflamatorios (el "fenotipo secretor asociado a senescencia"). En modelos animales, eliminar células senescentes con fármacos senolíticos mejora múltiples parámetros de salud y extiende healthspan. [[40]]
Pequeños estudios humanos piloto están en curso, pero no hay datos de eficacia o seguridad a largo plazo. La traslación de hallazgos animales a humanos en investigación de envejecimiento tiene historial decepcionante —muchas intervenciones prometedoras en roedores no se replican en humanos.
Reprogramación parcial, NAD+ boosters y metformina para longevidad:
Estas intervenciones generan titulares regulares. La reprogramación parcial es especulación teórica muy temprana. Los NAD+ boosters y metformina para longevidad tienen estudios en curso, sin conclusiones definitivas.
Conviene una posición editorial clara: hasta que existan ensayos clínicos aleatorizados en humanos de duración adecuada (idealmente décadas) con outcomes de healthspan como endpoints primarios, estas intervenciones no tienen lugar en recomendaciones prácticas. La curiosidad científica es legítima; la adopción prematura no lo es.
Límites biológicos del healthspan
No sabemos si existe un límite superior "duro" al healthspan humano. La heterocronia —diferentes tejidos envejecen a ritmos distintos— complica el objetivo de "rejuvenecimiento" coordinado. Algunos sistemas pueden ser más plásticos que otros.
Esta incertidumbre fundamental sobre límites biológicos debe informar nuestras expectativas. La compresión de morbilidad es alcanzable dentro de rangos documentados. La extensión radical de healthspan más allá de lo observado en poblaciones humanas actuales permanece especulativa. Esta línea entre lo alcanzable y lo especulativo merece trazarse con precisión.
Aplicación práctica: qué puedes hacer con este conocimiento
Las orientaciones siguientes se basan en evidencia observacional robusta (Nivel B), pero no garantizan resultados individuales específicos. El healthspan depende de múltiples factores, muchos fuera del control individual. Esta sección no sustituye asesoramiento médico personalizado.
Prioridades con mejor respaldo evidencial
1. Movimiento regular y progresivo
Cardio más entrenamiento de fuerza muestra la asociación más fuerte con compresión de morbilidad. Las guías OMS sugieren 150+ minutos semanales de actividad moderada más dos sesiones de resistencia. Esta no es una recomendación universal —requiere tiempo, acceso a espacios seguros, ausencia de limitaciones físicas previas. Pero para quienes tienen acceso, la evidencia es consistente.
2. Patrón alimentario no procesado
No hay dieta única "óptima." La consistencia en evidencia existe para patrones mediterráneos, DASH, y plant-forward. El denominador común: minimizar ultraprocesados. Esto requiere acceso a alimentos frescos y tiempo para prepararlos —recursos desigualmente distribuidos.
3. Sueño consistente
7-8 horas por noche con regularidad. Esto no es trivial —requiere control sobre horarios laborales y ausencia de trastornos del sueño no tratados.
4. No tabaco, alcohol limitado
La evidencia para tabaco es más clara que para casi cualquier otro factor. Para alcohol, la posición más conservadora tiene mejor respaldo actual: si no bebes, no hay razón para empezar; si bebes, limitar.
5. Conexión social significativa
Las asociaciones con supervivencia y funcionalidad son tan fuertes como factores físicos. La soledad y el aislamiento son riesgos de salud pública subestimados.
Grado de evidencia general: B (asociaciones fuertes en estudios observacionales, causalidad inferida razonablemente pero no definitiva)
Qué no tiene sentido hacer
- No perseguir biomarcadores no validados —telómeros comerciales, "edad biológica" sin contexto clínico.
- No asumir que suplementos "anti-aging" tienen evidencia —la mayoría no la tiene.
- No extrapolar estudios animales a decisiones personales.
- No confiar en promesas de "añadir X años de vida saludable" con intervención única —esas afirmaciones exceden la evidencia disponible.
Desconfia de cualquier narrativa que simplifique healthspan a una fórmula simple. La realidad es estructuralmente compleja.
Reorientando el objetivo: de vivir más a vivir mejor
El cambio de métrica que importa
El objetivo racional no es maximizar años totales a cualquier costo, sino maximizar años funcionales. Esta distinción reorienta fundamentalmente cómo evaluamos progreso médico, decisiones de salud personal y políticas públicas.
Esto no devalúa vida con limitaciones —la calidad de vida es multidimensional y subjetiva, muchas personas con condiciones crónicas reportan satisfacción vital alta. Lo que reconoce es el valor de autonomía y la reducción de sufrimiento evitable.
El cambio de prioridad implica: de tratamiento tardío hacia prevención temprana y sostenida. De gestionar enfermedades establecidas hacia reducir su incidencia. De añadir años al final hacia añadir funcionalidad a los años.
Implicaciones para evaluación de intervenciones
Toda intervención en longevidad debería medirse por impacto en healthspan, no solo lifespan. La pregunta correcta no es "¿esto me hace vivir más?" sino "¿esto preserva funcionalidad hasta edad avanzada?"
Este marco evalúa el futuro contenido de Muana Lab. Cada artículo subsecuente sobre intervenciones específicas —ejercicio, nutrición, sueño, manejo de estrés— se ancla en esta distinción conceptual. Sin ella, carecemos de norte.
Conclusión: Certezas, incertidumbres y camino adelante
Lo que sabemos con certeza (Grado A):
- El gap healthspan-lifespan existe y está documentado globalmente con solidez epidemiológica. Vivimos más años, pero una proporción significativa de esos años transcurre con discapacidad funcional y enfermedad crónica. Este no es un destino biológico inevitable.
- La compresión de morbilidad es alcanzable —retrasar el inicio de declive funcional hacia etapas finales de vida está demostrado en subpoblaciones y estudios longitudinales robustos.
- Los determinantes sociales son tan importantes como elecciones individuales. El healthspan no es primariamente producto de "responsabilidad personal"—está profundamente estructurado por nivel socioeconómico, educación, acceso a recursos y factores ambientales.
Lo que es probable pero requiere matiz (Grado B):
- Factores modificables —ejercicio, patrón alimentario, sueño, no tabaco, conexión social— tienen asociación fuerte con mejor healthspan en estudios observacionales. La causalidad es inferida razonablemente pero no definitiva. La magnitud exacta del efecto y la aplicabilidad individual permanecen inciertos.
- Intervenciones médicas preventivas —control de presión arterial, glucosa, lípidos; vacunación; screening oncológico selectivo— reducen morbilidad específica. El impacto agregado en healthspan total requiere inferencia desde datos de mortalidad y eventos, menos frecuentemente desde funcionalidad mantenida.
Lo que aún no sabemos (Grado C):
- Los límites biológicos del healthspan humano permanecen inciertos. No sabemos si existe un techo "duro" más allá del cual la compresión de morbilidad no puede avanzar, o si ese límite es más plástico de lo que actualmente comprendemos.
- Biomarcadores predictivos individuales —relojes epigenéticos, perfiles proteómicos— son prometedores en investigación pero carecen de validez clínica establecida para modificar decisiones.
- Intervenciones emergentes— senolytics, reprogramación parcial, NAD+ boosters— generan hipótesis interesantes en modelos animales pero no tienen evidencia humana de eficacia o seguridad a largo plazo.
La postura de Muana Lab:
Optimismo basado en evidencia sólida, no especulación. Reconocimiento de límites actuales sin nihilismo. Este artículo establece el marco conceptual —los siguientes profundizarán en intervenciones específicas con el mismo rigor.
La distinción healthspan-lifespan no es un tecnicismo semántico. Es la brújula que orienta todo lo que sigue. Sin claridad sobre qué estamos intentando optimizar, cualquier conversación sobre longevidad carece de sentido preciso.
Hasta aquí llega lo que sabemos con certeza suficiente. Lo que sigue requiere investigación continua, honestidad sobre incertidumbres y resistencia a promesas prematuras. Esa es la posición desde la cual Muana Lab construye su archivo editorial.
Preguntas frecuentes sobre healthspan y lifespan
¿Qué diferencia hay entre healthspan y lifespan?
El lifespan es el número total de años vividos desde el nacimiento hasta la muerte. El healthspan es el subconjunto de esos años vividos con funcionalidad plena, sin enfermedad crónica mayor ni discapacidad significativa. A nivel global, la diferencia promedio es de 9,6 años. Comprender esta distinción es el punto de partida de cualquier enfoque racional sobre longevidad.
¿Cuántos años de vida saludable perdemos de media?
Según datos de la OMS de 2019, la esperanza de vida global era de 73,3 años y la esperanza de vida saludable (HALE) de 63,7 años — una brecha de 9,6 años. En países de ingresos altos, esta brecha tiende a ser mayor. Entre 1990 y 2019, los años vividos con discapacidad aumentaron un 34% a nivel mundial.
¿Se puede reducir el tiempo vivido con enfermedad crónica?
Sí, y hay evidencia longitudinal robusta que lo demuestra. El concepto se llama compresión de morbilidad. El Harvard Alumni Health Study documentó un retraso medio de 5 años en el inicio de discapacidad en personas con actividad física regular y sin tabaquismo. El efecto poblacional es consistente, aunque sin garantía individual.
¿Qué factores tienen más evidencia científica para mejorar el healthspan?
La evidencia más sólida (estudios observacionales de largo plazo) señala cinco factores: ejercicio regular combinando cardio y entrenamiento de fuerza, patrón alimentario no ultraprocesado, sueño consistente de 7–8 horas, no fumar, y conexión social significativa. La causalidad es razonablemente inferida, no definitiva.
¿Los biomarcadores de «edad biológica» sirven para medir el healthspan?
Actualmente no de forma clínicamente útil. Los relojes epigenéticos y la longitud telomérica tienen valor como herramientas de investigación, pero no existe un biomarcador validado individualmente que justifique cambiar decisiones clínicas más allá de factores tradicionales como presión arterial, glucosa o lípidos.
¿Vivir más años siempre mejora el healthspan?
No necesariamente. El aumento de longevidad puede acompañarse de más años con enfermedad crónica controlada pero no curada. La medicina del siglo XX redujo la mortalidad aguda pero generó más décadas de multimorbilidad gestionada farmacológicamente. El objetivo no es maximizar años totales sino maximizar años funcionales.
¿Cuánto influye la genética frente al estilo de vida en el healthspan?
La genética establece una predisposición, no un destino. Estudios de gemelos sugieren que la genética explica entre el 25–30% de la variabilidad en longevidad; el resto es atribuible a factores ambientales y de estilo de vida. El margen de influencia individual es significativo, aunque no ilimitado ni igual para todos los contextos socioeconómicos.
¿Por qué los suplementos antiaging no tienen evidencia sólida para el healthspan?
Porque no existen ensayos clínicos de décadas de duración con funcionalidad como endpoint primario para ningún suplemento. La mayor parte de la investigación proviene de modelos animales. La extrapolación de roedores a humanos tiene un historial decepcionante en investigación del envejecimiento.
¿Qué diferencia hay entre healthspan y «calidad de vida»?
El healthspan es más preciso y objetivo: se mide con indicadores validados como capacidad para actividades básicas de forma independiente (ADL/IADL) y ausencia de multimorbilidad severa. La calidad de vida incluye satisfacción vital, propósito y relaciones — conceptos subjetivos que no siempre correlacionan directamente con el healthspan funcional.
¿A partir de qué edad tiene sentido preocuparse por el healthspan?
Desde la edad adulta joven. Las trayectorias de salud que determinan el healthspan a los 70–80 años se establecen con décadas de anticipación. Los factores de riesgo acumulados durante los 30–50 años tienen efectos compuestos sobre la funcionalidad posterior.
Disclaimer • Todo el contenido de Muana Lab —artículos, guías, informes y cualquier otro material— tiene carácter exclusivamente informativo. No pretende sustituir el consejo, diagnóstico ni tratamiento de un profesional sanitario cualificado. Ante cualquier duda sobre tu salud, consulta siempre con tu farmacéutico y/o médico u otro profesional competente. Muana Lab no recomienda la suplementación nutricional en sustitución del consejo o tratamiento médico adecuado. Si tomas medicación prescrita o sigues un tratamiento médico activo, consulta con tu farmacéutico antes de incorporar cualquier suplemento o cambio en tu pauta nutricional. Muana Lab no asume responsabilidad por las decisiones tomadas a partir de la información publicada ni por efectos secundarios imprevistos, incluso a dosis habituales. La mención de productos, sustancias o intervenciones no implica recomendación ni aval de su uso.
[[1]]: GBD 2021 Diseases and Injuries Collaborators. Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet. 2020;396(10258):1204-1222. doi:10.1016/S0140-6736(20)30925-9.
[[2]]: World Health Organization. Global Health Estimates: Life expectancy and leading causes of death and disability. Geneva: WHO; 2021.
[[3]]: GBD 2019 Diseases and Injuries Collaborators. Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet. 2020;396(10258):1204-1222. doi:10.1016/S0140-6736(20)32226-1
[[4]]: Vasan RS, Xanthakis V, Lyass A, et al. Epidemiology of cardiovascular disease in elderly individuals: Framingham Heart Study contributions. J Geriatr Cardiol. 2013;10(1):1-8. doi:10.1016/j.jcmg.2017.08.007
[[5]]: Barnett K, Mercer SW, Norbury M, et al. Epidemiology of multimorbidity and implications for health care, research, and medical education: a cross-sectional study. Lancet. 2012;380(9836):37-43. doi:10.1016/S0140-6736(12)60240-2
[[6]]: Crimmins EM, Zhang Y, Saito Y. Trends over 4 decades in disability-free life expectancy in the United States. Am J Public Health. 2016;106(7):1287-1293. doi:10.2105/AJPH.2016.303120
[[7]]: Stringhini S, Carmeli C, Jokela M, et al. Socioeconomic status and the 25×25 risk factors as determinants of premature mortality: a multicohort study and meta-analysis of 1.7 million men and women. Lancet. 2017;389(10075):1229-1237. doi:10.1016/S0140-6736(16)32380-7
[[8]]: Oksuzyan A, Juel K, Vaupel JW, Christensen K. Men: good health and high mortality. Sex differences in health and aging. Aging Clin Exp Res. 2008;20(2):91-102. doi:10.1007/BF03324754
[[9]]: Robine JM, Cubaynes S. Worldwide demography of centenarians. Mech Ageing Dev. 2017;165(Pt B):59-67. doi:10.1016/j.mad.2017.03.004
[[10]]: Yeh RW, Sidney S, Chandra M, et al. Population trends in the incidence and outcomes of acute myocardial infarction. N Engl J Med. 2010;362(23):2155-2165. doi:10.1056/NEJMoa0908610
[[11]]: Buttorff C, Ruder T, Bauman M. Multiple Chronic Conditions in the United States. Santa Monica, CA: RAND Corporation; 2017.
[[12]]: Dugravot A, Fayosse A, Dumurgier J, et al. Social inequalities in multimorbidity, frailty, disability, and transitions to mortality: a 24-year follow-up of the Whitehall II cohort study. Lancet Public Health. 2020;5(1):e42-e50. doi:10.1016/S2468-2667(19)30226-9
[[13]]: World Health Organization. Obesity and overweight. Fact sheet. Geneva: WHO; 2021. doi:10.4236/ojapps.2023.138110
[[14]]: Guthold R, Stevens GA, Riley LM, Bull FC. Worldwide trends in insufficient physical activity from 2001 to 2016: a pooled analysis of 358 population-based surveys with 1.9 million participants. Lancet Glob Health. 2018;6(10):e1077-e1086. doi:10.1016/S2214-109X(18)30357-7
[[15]]: Srour B, Fezeu LK, Kesse-Guyot E, et al. Ultra-processed food intake and risk of cardiovascular disease: prospective cohort study (NutriNet-Santé). BMJ. 2019;365:l1451. doi:10.1136/bmj.l1451
[[16]]: Li Y, Pan A, Wang DD, et al. Impact of healthy lifestyle factors on life expectancies in the US population. Circulation. 2018;138(4):345-355. doi:10.1161/CIRCULATIONAHA.117.032047
[[17]]: Stringhini S, Sabia S, Shipley M, et al. Association of socioeconomic position with health behaviors and mortality. JAMA. 2010;303(12):1159-1166. doi:10.1001/jama.2010.297
[[18]]: Sallis JF, Floyd MF, Rodríguez DA, Saelens BE. Role of built environments in physical activity, obesity, and cardiovascular disease. Circulation. 2012;125(5):729-737. doi:10.1161
[[19]]: Paffenbarger RS Jr, Hyde RT, Wing AL, et al. The association of changes in physical-activity level and other lifestyle characteristics with mortality among men. N Engl J Med. 1993;328(8):538-545. doi:10.1056/NEJM199302253280804
[[20]]: Li Y, Schoufour J, Wang DD, et al. Healthy lifestyle and life expectancy free of cancer, cardiovascular disease, and type 2 diabetes: prospective cohort study. BMJ. 2020;368:l6669. doi:10.1136/bmj.l6669
[[21]]: Crimmins EM, Beltrán-Sánchez H. Mortality and morbidity trends: is there compression of morbidity? J Gerontol B Psychol Sci Soc Sci. 2011;66(1):75-86. doi:10.1093/geronb/gbq088
[[22]]: Ekelund U, Tarp J, Steene-Johannessen J, et al. Dose-response associations between accelerometry measured physical activity and sedentary time and all cause mortality: systematic review and harmonised meta-analysis. BMJ. 2019;366:l4570. doi:10.1136/bmj.l4570
[[23]]: Westcott WL. Resistance training is medicine: effects of strength training on health. Curr Sports Med Rep. 2012;11(4):209-216. doi:10.1249/JSR.0b013e31825dabb8
[[24]]: World Health Organization. WHO guidelines on physical activity and sedentary behaviour. Geneva: WHO; 2020. doi:10.1136/bjsports-2020-102955
[[25]]: Estruch R, Ros E, Salas-Salvadó J, et al. Primary prevention of cardiovascular disease with a Mediterranean diet supplemented with extra-virgin olive oil or nuts. N Engl J Med. 2018;378(25):e34. doi:10.1056/NEJMoa1800389
[[26]]: Sacks FM, Svetkey LP, Vollmer WM, et al. Effects on blood pressure of reduced dietary sodium and the Dietary Approaches to Stop Hypertension (DASH) diet. N Engl J Med. 2001;344(1):3-10. doi:10.1056/NEJM200101043440101
[[27]]: Satija A, Bhupathiraju SN, Spiegelman D, et al. Healthful and unhealthful plant-based diets and the risk of coronary heart disease in U.S. adults. J Am Coll Cardiol. 2017;70(4):411-422. doi:10.1016/j.jacc.2017.05.047
[[28]]: Ungvari Z, Fekete M, Varga P, et al. Imbalanced sleep increases mortality risk by 14-34%: a meta-analysis. GeroScience. 2025;47. doi:10.1007/s11357-025-01592-y
[[29]]: Jha P, Ramasundarahettige C, Landsman V, et al. 21st-century hazards of smoking and benefits of cessation in the United States. N Engl J Med. 2013;368(4):341-350. doi:10.1056/NEJMsa1211128
[[30]]: Wood AM, Kaptoge S, Butterworth AS, et al. Risk thresholds for alcohol consumption: combined analysis of individual-participant data for 599,912 current drinkers in 83 prospective studies. Lancet. 2018;391(10129):1513-1523. doi:10.1016/S0140-6736(18)30134-X
[[31]]: Holt-Lunstad J, Smith TB, Layton JB. Social relationships and mortality risk: a meta-analytic review. PLoS Med. 2010;7(7):e1000316. doi: 10.1371/journal.pmed.1000316
[[32]]: Ettehad D, Emdin CA, Kiran A, et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet. 2016;387(10022):957-967. doi: 10.1016/S0140-6736(15)01225-8
[[33]]: Cholesterol Treatment Trialists' (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet. 2010;376(9753):1670-1681. doi:10.1016/S0140-6736(10)61350-5
[[34]]: UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837-853.
[[35]]: Jackson ML, Chung JR, Jackson LA, et al. Influenza vaccine effectiveness in the United States during the 2015-2016 season. N Engl J Med. 2017;377(6):534-543. doi:10.1056/NEJMoa1700153
[[36]]: Zauber AG, Winawer SJ, O'Brien MJ, et al. Colonoscopic polypectomy and long-term prevention of colorectal-cancer deaths. N Engl J Med. 2012;366(8):687-696. doi:10.1056/NEJMoa1100370
[[37]]: Independent UK Panel on Breast Cancer Screening. The benefits and harms of breast cancer screening: an independent review. Lancet. 2012;380(9855):1778-1786. doi:10.1038/bjc.2013.177
[[38]]: Haycock PC, Heydon EE, Kaptoge S, et al. Leucocyte telomere length and risk of cardiovascular disease: systematic review and meta-analysis. BMJ. 2014;349:g4227. doi:10.1136/bmj.g4227
[[39]]: Horvath S. DNA methylation age of human tissues and cell types. Genome Biol. 2013;14(10):R115. doi:10.1186/gb-2013-14-10-r115
[[40]]: Xu M, Pirtskhalava T, Farr JN, et al. Senolytics improve physical function and increase lifespan in old age. Nat Med. 2018;24(8):1246-1256. doi:10.1038/s41591-018-0092-9







Discussion